Niels Bohr nació el 7 de Octubre de 1885, dentro de una familia progresista descrita como agradable. Su padre era profesor de fisiología, y estuvo a punto de ganar un premio Nobel.
Niels Bohr nació el 7 de Octubre de 1885, dentro de una familia progresista descrita como agradable. Su padre era profesor de fisiología, y estuvo a punto de ganar un premio Nobel.Fue un joven callado y tímido, de aspecto algo torpe. Era un alumno aventajado, que además jugaba al fútbol, al igual que su hermano Harald, un año menor que Niels. Su hermano era una de las personas más importantes de su vida. Nunca se separaban.
Sin embargo, su hermano destacó por encima de Niels como alumno en matemáticas y como futbolista. A pesar de ello, no hubo rivalidades entre los dos.
Su hermana mayor Jenny también fue una gran estudiante y se convirtió en una gran profesora. Sin embargo, debido a un problema nervioso fue ingresada en un manicomio, donde murió.
En 1903 los dos hermanos entraron en la universidad de Copenhague, en una época de cambios y avances científicos. Entraron en el equipo de fútbol de la universidad, y rápidamente adquirieron fama de genios entre sus compañeros.
En 1907 recibió un premio por un ensayo sobre la tensión superficial del agua. Los experimentos fueron apresurados coincidiendo con sus exámenes finales.
En la casa de los dos hermanos se organizan charlas filosóficas en las que participan como oyentes, lo cual influye en los pensamientos, incluso científicos, de Niels.
Bohr desea reducir el lenguaje a una estructura lógica precisa, aclarando la ambigüedad al nombrar el plano de objetividad. Realiza interpretaciones filosóficas.
Muchos científicos rechazan el pensamiento y apoyan la experimentación. Por ello, la existencia del átomo se cuestiona en aquel entonces ya que nadie había conseguido observar ninguno. La relatividad, en cambio, se descubre gracias al pensamiento.
Bohr realiza su tesis doctoral como un trabajo teórico.
En 1987 Thomson descubre la existencia del electrón, lo que confirma la existencia del átomo. Algunos científicos, como Mach, siguen rechazando estas ideas.
Las teorías que surgen son provisionales y sin suficientes fundamentos. Bohr opina que la teoría clásica no da explicaciones a niveles subatómicos.
Viaja hasta Cambridge para investigar junto a Bohr en 1911. No es bien acogido, debido en gran parte a falta de claridad al expresarse. Bohr intenta mejorar su inglés. Thomson le desprecia.
Bohr persevera en su idea de la existencia de otra física distinta de la clásica.
En una cena en honor a Rutherford los dos científicos se conocen, congeniando muy bien. Rutherford invita a Bohr a trabajar con él en Manchester y este acepta. A pesar de ser dos científicos opuestos no tienen problemas. Rutherford basa sus teorías en la práctica, pero acepta las teorías de Bohr debido a que las considera brillantes.
Rutherford experimenta con partículas subatómicas creando un nuevo modelo atómico. Dedujo la existencia de un núcleo atómico positivo a través de sus experimentos. Bombardeo una lámina de oro con partículas alfa, observando la mayoría de las partículas la atravesaba, algunas eran desviadas y otras rechazadas. El núcleo positivo se encuentra en el centro y los electrones giran a su alrededor. Cuando las partículas chocan contra el núcleo o lo rozan son rechazadas o desviadas.
Aunque el modelo de Rutherford rechaza las leyes clásicas, da explicación a numerosas cuestiones. Hasta el siglo XIX todo había sido explicado por la física clásica.
En 1900 Planck descubre el primer paso contra la física clásica. La radiación se forma de ondas-partículas. Las ondas no son continuas, sino que se emiten por cuantos. Einstein más tarde confirma la teoría de Planck a través del efecto fotoeléctrico.
La ciencia sigue negando estas teorías. No se encuentra relación entre las teorías de Einstein, Bohr y el modelo de Rutherford.
Un maestro de escuela, descubre una fórmula para los espectros de emisión de los Balmer, gases con la que se obtiene la longitud de onda.
Bohr estudia el modelo de Rutherford y descubre la relación entre la fórmula de Balmer, la teoría cuántica y el modelo de Rutherford.
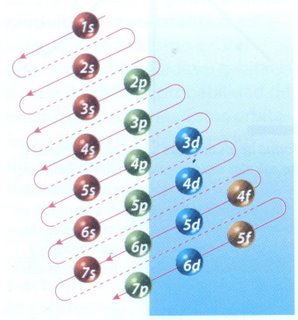
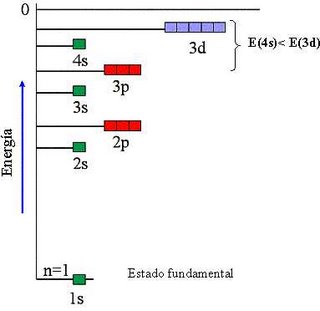
Estudia el hidrógeno, cuyo electrón podía describir órbitas diferentes. Al pasar de una órbita a otra el electrón emite energía. Cuando el electrón mantiene una órbita fija se encuentra en su estado estacionario. La energía emitida conforma el espectro. En cada órbita el radio del electrón es diferente. La diferencia entre radios da la diferencia entre estados energéticos.
La nueva física comienza a explicar los fenómenos subatómicos.
Bohr sigue estudiando la estructura atómica ya que quiere encontrar un respaldo al modelo de Rutherford.
Vuelve a Dinamarca en 1912 donde conoce a Margarethe, de la que se enamora. Finalmente se casan ese año.
Bohr es nombrado profesor en Copenhague posteriormente. Mantiene correspondencia con Rutherford, quien revisa sus escritos.
En 1913 publica un artículo que causa sensación, donde sugería que la teoría cuántica era la manera de funcionar de los átomos. Algunos tachan sus ideas de tonterías ya que el modelo no explicaba algunos detalles.
Un científico llamado Arnold Sommerfeld aplicó la relatividad a los electrones, deduciendo que sus órbitas eran elípticas.
En 1914 Rutherford ofrece a Bohr otro puesto en Manchester. Bohr trata de extender su modelo al plan general de las estructuras atómicas.
Al comenzar la 1ª Guerra Mundial las comunicaciones se dificultan, aunque no se imposibilitan.
Bohr se embarca en unos experimentos para comprobar unas teorías alemanas relacionadas con sus teorías. Para ello, son necesarias delicadas precias de cristal. Consiguieron que un hombre alemán especializado en la creación de dichas piezas, trabajase en Inglaterra durante la guerra. Tras provocar algunos incidentes, el hombre fue detenido. En un incendio, el experimento es destruido y Bohr no llega a finalizarlo.
Nace su primer hijo en 1916.
Dinamarca quiere recuperar al científico, y lo consiguen ofreciéndole una cátedra y fondos para crear su propio instituto de investigación. El ambiente de camaradería del laboratorio de Rutherford influirán en la dirección del suyo propio. En 1918 comienzan las obras.
Jóvenes científicos acuden al instituto y se realizan numerosos avances. Se descubre un nuevo elemento, el hafnio. Arthur Scott declara que él lo había ya descubierto, pero finalmente se demuestra que no es cierto.
Bohr recibe el premio Nobel de física en 1922.
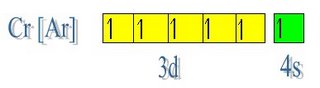
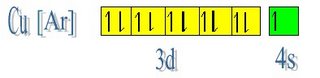
Poco después de ello, Bohr formula su principio de correspondencia. Descubre que el átomo puede ser clásico o cuántico. Las leyes de la teoría cuántica y la mecánica clásica son idénticas a bajas frecuencias. El descubrimiento resulta confuso incluso para el propio Bohr. El modelo de Bohr se iba ampliando. Podía mostrar ya la disposición de los electrones en átomos más complejos. Sin embargo, algunas cuestiones aún no poseían explicación. La órbita interna de los electrones, según el esquema de Bohr, debía acabar saturándose, y no era así. Un alumno del instituto, Pauli, encuentra la explicación. Dedujo que los electrones giran sobre sí mismos, además de alrededor del núcleo. Esto explicó también la estructura de los elementos en la tabla periódica.
Aunque Bohr no participa directamente en estos avances, si lo hace indirectamente gracias al ambiente fructífero que crea en su instituto.
Werner Heisenberg realiza otro avance en 1925 al encontrar explicación al principio de correspondencia de Bohr. Aunque pareciese imposible que la cuántica y la física clásica coincidiesen a bajas frecuencias, Heisenberg decide que debe centrarse en las mediciones, ya que los resultados deberían ser similares a pesar de q parezca imposible. Dispone las mediciones en forma de matriz. Así postula su principio de indeterminación, que afirma que cualquier observación o intento de medición del electrón afectará mínimamente a este. Solo puede trabajarse con probabilidades.
Bohr declara en su principio de complementariedad que el comportamiento del electrón como una onda o una partícula dependerá del aparato utilizado en la medición.
Bohr inicia una serie de conferencias en 1929 donde se discuten diversas cuestiones científicas. No se consiguen respuestas unánimes, pero se intentan resolver. Es una época de grandes conferencias científicas.
Algunos científicos como Schröndinger rechazan la mecánica cuántica. Ataca el enfoque probabilístico de la predicción en la cuántica a través de su ejemplo conocido como “el gato de Schrödinger”.
Bohr aplica su principio de complementariedad a otros aspectos cotidianos, incluso a la filosofía. Nadie considera a Bohr dotado para ello.
En los años 30 estudia el núcleo del átomo. En esa misma época, otros dos científicos, Otto Hahn y Lise Meitner, descubren la fisión nuclear. Bohr es informado de ello, y se lo advierte a Einstein, quien a su vez se lo comunica al presidente Rooselvelt. Surge el proyecto Manhattan y crean la bomba atómica norteamericana.
Heisenberg participo en el proyecto alemán. Bohr y él no conservan buena relación.
Dinamarca es invadida, y en 1943 Bohr es perseguido por los nazis, y huye con su familia a Estocolmo. Los alemanes ordenan asesinarle. El gobierno británico le ayuda a escapar, proporcionándole un avión. Viaja hasta Estados Unidos, donde participa en el proyecto Manhattan.
Tras el lanzamiento de las bombas atómicas, Bohr queda horrorizado con los resultados, y desde entonces intenta utilizar su influencia para detener las investigaciones sobre bombas atómicas.
Tras la muerte de Einstein, se le considera el mayor científico vivo.
Muere en 1962 a los 77 años.
DESCUBRIMIENTOS CIENTÍFICOS
- En 1897 Thomson descubre la existencia del electrón. Realiza un modelo atómico donde supone que los electrones se encuentran incrustados a una masa de carga positiva. Teoría del electrón en los metales.
- Experimento de Rutherford con partículas subatómicas: bombardea una lámina de oro con partículas alfa. La mayoría de estas partículas atraviesa la lámina sin desviarse, otras se desvían parcialmente, y otras son rechazadas.
- El modelo atómico de Rutherford surge a partir de la interpretación de dicho experimento. Dedujo la existencia de un núcleo positivo, alrededor del cuál, los electrones giran en órbitas circulares.
- Surge la teoría cuántica de Planck en 1900: la radiación se forma de ondas-partículas, los cuantos. Las ondas no son continuas, sino que están formadas por cuantos. El tamaño de los cuantos varía en proporción de la frecuencia.
- Einstein explica la teoría cuántica a través del efecto fotoeléctrico: la luz ultravioleta alcanza a ciertos metales provocando una emisión de electrones. Su nivel de emisión depende de la frecuencia y no de la intensidad. Esto se explica si la luz se compone de cuantos.
- El electroscopio es inventado en 1814 por Joseph Von Fraunhofer, gracias a lo que es posible observar las estructuras de los elementos.
- Un maestro de escuela llamado Johann Balmer descubre en 1885 la formula del espectro de emisión de los gases.
- Bohr relaciona la fórmula de Balmer y la teoría cuántica, creando un modelo atómico: el electrón permanece en su estado estacionario si mantiene una órbita fija, pero si se mueve entre las órbitas, emitirá energía. Esa energía constituía las distintas bandas de emisión.
- Arnold Sommerfeld aplicó la relatividad a los electrones, deduciendo que sus órbitas eran elípticas.
- Se descubre un nuevo elemento en los primeros años de existencia del instituto de Bohr, el hafnio.
- Bohr formula su principio de correspondencia: las leyes de la teoría cuántica y la física clásica son idénticas a bajas frecuencias. El átomo puede ser clásico o cuántico.
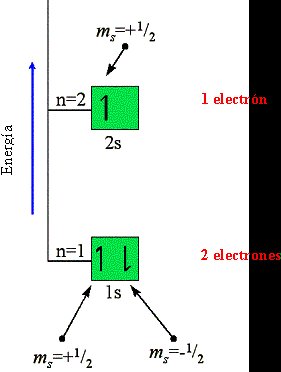
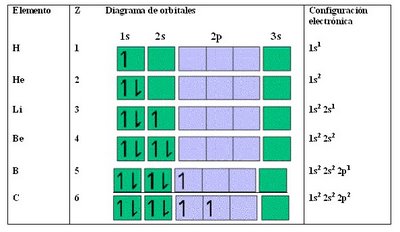
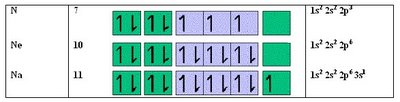
- En 1924 Pauli enuncia su principio de exclusión: los electrones giran sobre sí mismos, además de alrededor del núcleo. Explicaba porque los electrones no se amontonaban y la estructura de los elementos de la tabla periódica. No puede haber más de dos electrones en una órbita.
- Werner Heisenberg encuentra en 1925 explicación al principio de correspondencia de Bohr y postula su principio de indeterminación. Aunque la teoría de Bohr parezca increíble, debemos basarnos en las mediciones, pero la mecánica cuántica no ofrece una certeza total a pesar de su medición, ya que cualquier observación o medición del electrón afectara a su comportamiento.
- En 1927 Bohr postula su principio de complementariedad que explica que el comportamiento del electrón como onda o como partícula dependerá del aparato utilizado para su medición.
- Bohr presenta un modelo atómico que describe su composición y funcionamiento.
- Dos científicos, Otto Hahn y Lise Meitner, descubre en 1939 la fisión nuclear. El núcleo del átomo se descompone cuando la energía que provoca una partícula al chocar con él provoca una concentración de energía sobre otra partícula que permite a esta escapar. En los núcleos grandes la partícula que escapa provoca la división en dos mitades. Este proceso genera una gran energía.
ANÉCDOTAS
- El padre de Bohr, profesor de fisiología, casi ganó el premio Nobel.
- Niels era muy torpe, y acostumbraba a provocar accidentes en los laboratorios. En una ocasión, al escuchar una explosión procedente de los laboratorios, un profesor suyo dijo: “Ese debe de ser Bohr”.
- Los dos hermanos Bohr jugaban al fútbol en el equipo de la universidad. Harald llegó a jugar en los juegos olímpicos. Bohr era portero, y se dedicaba a hacer cálculos matemáticos en las porterías mientras el juego se desarrollaba en el otro extremo.
- Rutherford también fue jugador de rugby.
- Bohr tenía problemas para expresarse y para hablar francés e inglés. En una ocasión saludo al embajador francés con un cordial “Aujourd'hui” (Hoy).
- El inventor del electroscopio fue un óptico que sobrevivió al derrumbamiento del edificio donde trabajaba. El elector Maximiliano José conmemoró su salvación recompensándole, lo que le permitió a este dedicarse a la investigación.
- Cuando Bohr se traslada a Manchester en 1912 otro gran pensador de la época, el filósofo Wittgenstein, viajaba en el sentido contrario, trasladándose de Manchester a Cambridge.
- Rutherford solía ir cantando por sus laboratorios “Onward Christian Soldiers” (adelante soldados de Cristo).
- Algunos científicos rechazaron las ideas de Bohr. Max von Laue dijo en una ocasión: “Si esta teoría es correcta, abandonaré la física”. Finalmente no lo hizo, y llego a ser incluso íntimo amigo de Bohr.
- Bohr fue una persona informal. En una ocasión, en una audiencia con el rey, Bohr le contradijo cuando el rey pensó que se trataba de Bohr el futbolista. Niels le corrigió diciéndole que era su hermano. Según las reglas del protocolo, contradecir al rey está prohibido. Este le volvió a decir lo mismo para que Bohr rectificase, pero no lo hizo.
- Los fondos iniciales para el instituto de Bohr fueron aportados por Calsberg, una importante marca de cerveza danesa.
- En la época que Bohr recibía el premio Nobel también lo recibieron en un periodo de siete años Planck, Einstein, Milikan y Hertz, además de Bohr.
- Casi todos los grandes científicos de la época trabajaron en el instituto de Bohr.
- La conferencia científica más famosa, Solvay, se realizaba en el hotel Metropol de Bruselas, donde Bohr defendía sus ideas ante Einstein o Madame Curie, que pensaban que la cuántica era un fenómeno pasajero.
- Bohr era un pésimo conductor y su mujer debía sujetar el volante en algunas ocasiones para evitar posibles accidentes.
- Una historia cuenta que Bohr, queriendo evitar que su premio Nobel cayera en manos nazis, disolvió la medalla en ácido y la escondió, para más tarde volver a refundirla. La verdad fue que la medalla pertenecía a su amigo Von Laue.
- La mayoría de los ganadores del premio Nobel estaban en contra de los nazis, por lo que Hitler prohibió a los alemanes aceptar el premio Nobel al considerar a los anteriores ganadores de raza inferior.
- Su hijo Aage, con el que trabajo tras su vuelta de Estados Unidos, ganó más tarde un premio Nobel.
CONTEXTO SOCIAL Y POLÍTICO DE LA ÉPOCA.
Su juventud fue en una época de grandes progresos donde Europa dominaba el mundo. Los hermanos Bohr entran en la universidad en 1903, en una época de cambios: los hermanos Wright realizan su primer vuelo, y Marie Curie recibía el premio Nobel por su descubrimiento de la radioactividad.
En 1912, justo antes de que Bohr se trasladara a Manchester para trabajar con Rutherford, se desencadena la 1ªGuerra Mundial. Dinamarca permaneció neutral, pero Gran Bretaña se enfrentó a Alemania. Pese a la guerra, Bohr siguió recibiendo noticias de Alemania acerca de los progresos científicos que realizaban.
En una ocasión, un ayudante de Bohr para uno de sus pocos experimentos era alemán. Solo gracias al prestigio de Bohr consiguieron que pudiese trabajar en Inglaterra. El ayudante utilizaba cualquier momento posible para realizar discursos a favor de su nación. Finalmente fue detenido por algunos incidentes inflamatorios.
El siglo XX fue la época de mayores cambios y avances en la ciencia, y muchos de estos avances se produjeron en el instituto de Bohr. Fue una época de numerosas conferencias científicas donde los grandes científicos discutían numerosas cuestiones, en un ambiente de cooperación.
El descubrimiento de la fisión nuclear, realizado por un científico alemán y una científica judía(que tuvo que huir de la Alemania nazi durante el descubrimiento) puso en marcha el proyecto Manhattan con el fin de construir la bomba atómica. La información que proporciono Bohr sobre la fusión nuclear y su descubrimiento aceleró el proyecto con el fin de crear una bomba atómica norteamericana antes que Alemania.
 En 1940 Dinamarca fue invadida por los nazis. Bohr, debido a su declarado desprecio hacia los nazis, fue perseguido. Con la ayuda del gobierno británico llego hasta Estados Unidos, donde se unió al proyecto Manhattan. La cooperación científica internacional es en esta época encubierta.
En 1940 Dinamarca fue invadida por los nazis. Bohr, debido a su declarado desprecio hacia los nazis, fue perseguido. Con la ayuda del gobierno británico llego hasta Estados Unidos, donde se unió al proyecto Manhattan. La cooperación científica internacional es en esta época encubierta.Las primeras bombas atómicas estadounidenses son lanzadas en Japón en 1945, lo que supone el fin de la 2ª Guerra Mundial.
Durante la guerra, Hitler prohibió a los alemanes aceptar el premio Nobel ya que todos los premiados anteriormente rechazaban a los nazis, y eran considerados de raza inferior.
OPINIÓN PERSONAL
El autor muestra de una forma interesante la vida de uno de los grandes científicos del siglo XX científico. La fluidez del libro y sus anécdotas ayudan a entender mejor sus descubrimientos, que durante años hemos estudiado en las clases, y a ver descubrir el lado humano de los científicos que estudiamos. Podemos hacernos una idea de cómo fue la vida y la época en la que vivieron todos los científicos nombrados. Nos muestra la influencia de la ciencia en los acontecimientos de la historia de todo el mundo, siendo un claro ejemplo el descubrimiento de la fusión nuclear y con ellos la construcción de la bomba atómica.